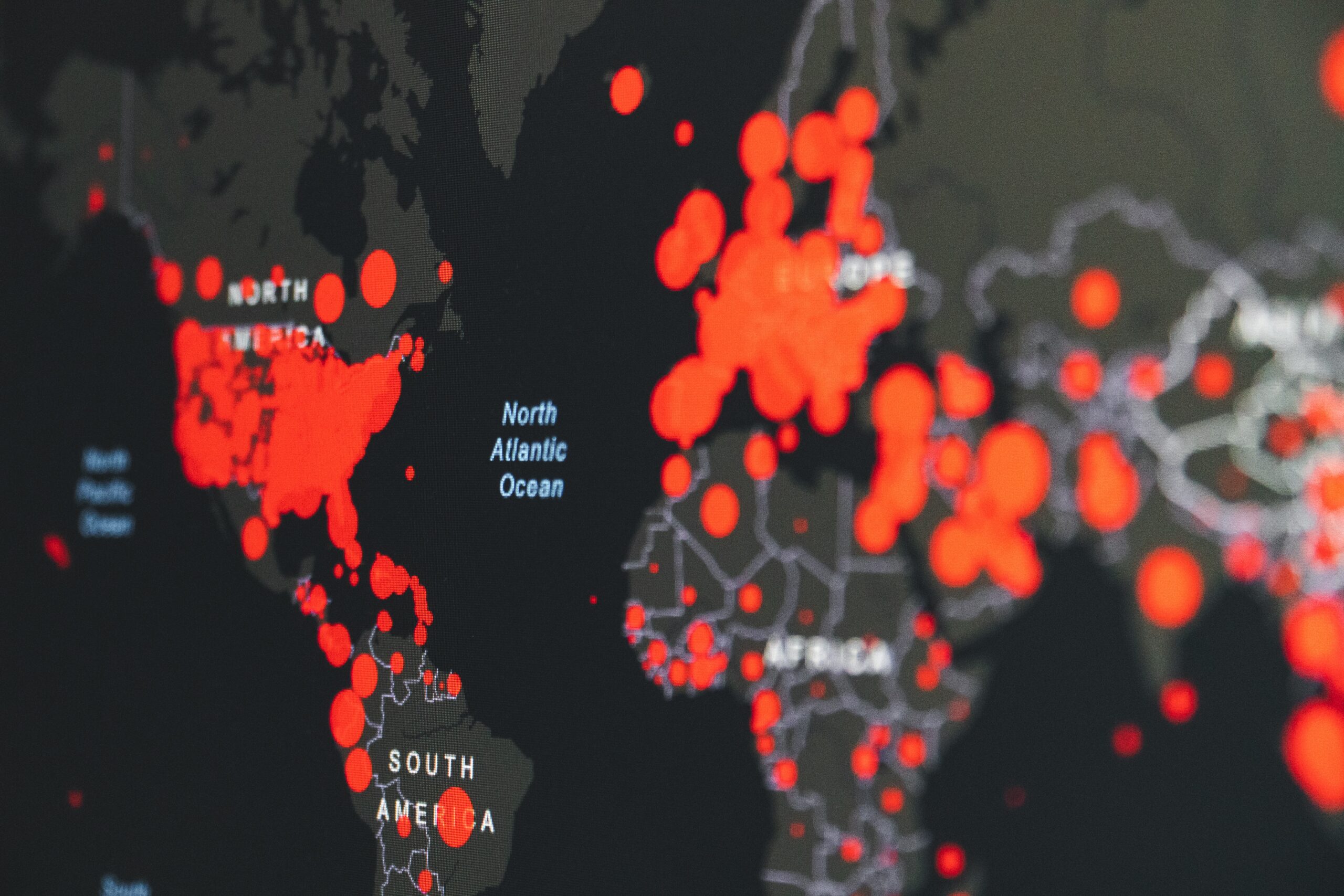
Pendant la pandémie du Covid-19, certaines populations ont semblé résister plus que d’autres au virus. Alors que l’OMS mettait en avant des raisons incongrues, une nouvelle étude française nous éclaire sur cette différence d’exposition. Elle démontre une grande variabilité génétique liée notamment à la géographie et au bagage immunitaire.
La pandémie du Covid-19 a mis en évidence une disparité entre les individus dans la gravité des symptômes dus au SRAS-CoV-2. En effet, tandis que certaines personnes ont lutté pour leur survie sur les lits d’hôpitaux, d’autres sont restées asymptomatiques au virus, voire immunisées. Cette différence dans la sévérité de l’infection a été également observée par les virologues au niveau des populations. Les groupes ethniques ne souffraient pas de la pandémie au même degré.
Les défenses immunitaires différentes d’une population à une autre
Pour comprendre cette inégalité devant le Covid-19, l’Unité de Génétique évolutive humaine de l’Institut Pasteur, dirigée par le généticien Lluis Quintana-Murci, a mené une étude sur les potentiels facteurs à l’origine de la diversité des réponses immunitaires face au SARS-CoV-2. Elle a réalisé des expériences dans lesquelles il s’agissait d’exposer au virus des cellules sanguines immunitaires issues de 222 donneurs sains d’Afrique centrale, d’Europe de l’Ouest et d’Asie de l’Est.
Les scientifiques français ont constaté que 900 gènes répondaient différemment au SARS-CoV-2 en fonction des populations. Ils attribuent en partie ces différences à l’existence d’une proportion variable de cellules immunitaires. Ce qui signifie que les défenses immunitaires d’un Européen, d’un Asiatique et d’un Africain ne sont pas les mêmes. En d’autres termes, ils ne sont pas égaux devant un même pathogène (ici en l’occurrence le SARS-CoV-2).
Un bagage immunitaire acquis au fil des générations
Les variations de cellules immunitaires seraient principalement dues à la composition cellulaire du sang, différente d’une population à une autre sur le globe. La composition cellulaire dépendrait à son tour des facteurs environnementaux tels que l’exposition au cytomégalovirus, une infection humaine de la famille des herpès, inoffensive la plupart du temps. Dans leur étude, les chercheurs notent que le taux d’infection à ce virus courant différait d’un groupe ethnique à un autre.
En effet, près de 99 % de la population d’Afrique centrale était séropositive pour le cytomégalovirus, contre 50 % de la population d’Asie de l’Est et 32 % des Européens. Ainsi, comme les individus ne vivent pas dans le même environnement, ils ne subissent pas le même niveau d’exposition aux mêmes pathogènes, à la fois individuellement et collectivement. Leur mémoire immunitaire s’est constituée au fil des générations dans une ère géographique en s’ajoutant au patrimoine génétique (héritée des parents et ascendants).
Possibilité de concevoir de nouveaux traitements personnalisés
Dans ce contexte, les chercheurs ont établi un lien entre l’héritage génétique de nos ancêtres néandertaliens et la réponse immunitaire des populations actuelles. Entre 1,5 et 2 % du génome des Européens et des Asiatiques d’aujourd’hui porteraient l’ADN de l’homme de Neandertal. Ce qui n’est pas le cas des Africains, qui appartiennent à une autre lignée. Les scientifiques de l’Institut Pasteur ont pu identifier des dizaines de mutations néanderthaliennes qui affectent notre réponse immunitaire au SARS-CoV-2.
Cette étude établit ainsi des liens entre les disparités démographiques et génétiques ainsi que les événements évolutifs passés. A l’image de la sélection naturelle ou du métissage néandertalien, ainsi que des réponses immunitaires ou risque de maladie dans chaque population. Les autorités sanitaires ont donc désormais des indices pour mettre en place des stratégies de médecine de précision qui permettront d’identifier les individus à risque ou pour concevoir de nouveaux traitements plus personnalisés en fonction du patrimoine génétique.